Főbb különbség: A diffúzió az a folyamat, amellyel a molekulák egy helyről a másikra mozognak és utaznak anélkül, hogy tömeges mozgást igényelnek. Az effúzió az a folyamat, amellyel a molekulák egy nagy lyukú helyről alacsony koncentrációra haladnak.
A diffúzió és az effúzió kifejezéseket sok tudományban használják, mint például a kémia, a fizika és a biológia. A kémiában a két kifejezés a gázok két tulajdonsága. Ez a kettő zavaró a sok ember számára, akik csak a gázok alapjait és tulajdonságait tanulják. A diffúzió és az effúzió két különböző kifejezést jelent, amelyek két különböző dolgot jelentenek, és nem használhatók fel egymással felcserélhető módon. A diffúzió arra utal, hogy a gázok képesek egymással összekeverni, míg az effúzió a gáz azon képességére utal, hogy egy kis csaplyukon haladhat. A diffúziót a szociológiában, a közgazdaságtanban és a pénzügyekben is használják az emberek, az ötletek és az értékek terjesztésére.
A diffúzió az a folyamat, amellyel a molekulák egy helyről a másikra mozognak és nem mozdulnak el. A diffúzió a molekulák mozgását vagy keverését eredményezi, csak kinetikus energiával. A „diffúzió” szó a „diffundere” (latin) szóból származik, ami „elterjedt”. A diffúzióban a molekulák állandó mozgási állapotban vannak, és kinetikus vagy termikus energiával meghajtva hajlamosak más molekulákhoz keverni, ami elválaszthatatlan keveréket eredményez. Vegyünk egy gyakorlati megközelítést, egy tartályt A és B szakaszokra osztunk egy szilárd partícióval; az első rész vízzel van feltöltve, míg a második szakasz vörös festékkel van feltöltve. Most, amikor a partíciót felemelik, a festék és a víz megpróbálja kitölteni az egész tartályt. Ezután a festék lassan a vízvörös színt idézi, ez a diffúzió.
A diffúzió a molekulákat a magasabb koncentrációs területről alacsonyabb koncentrációs területre váltja, ami az összes molekula keverékét eredményezi. A diffúzió leáll, ha az összes molekula egyenletesen eloszlik. A diffúzió nem korlátozódik a vízre, és a legjobban működik gáznemű állapotokban, ahol a molekulák több energiával és képességgel rendelkeznek más molekulákkal való keverésre. A diffúziónak két megközelítése van: fenomenológiai és atomista. A fenomenológiai megközelítés szerint a molekulák nagyobb koncentrációjú régiókból utaznak alacsonyabb koncentrációjú régiókba. Az atomisztikus megközelítésben a diffúziót a diffúziós részecskék véletlenszerű séta következtében tekintik meg, amelyben a diffúziót a hőenergia hajtja, ami összekeveri őket. A diffúzió fontos szerepet játszik a szervezet által igényelt ásványi anyagok, tápanyagok és energia létrehozásában.

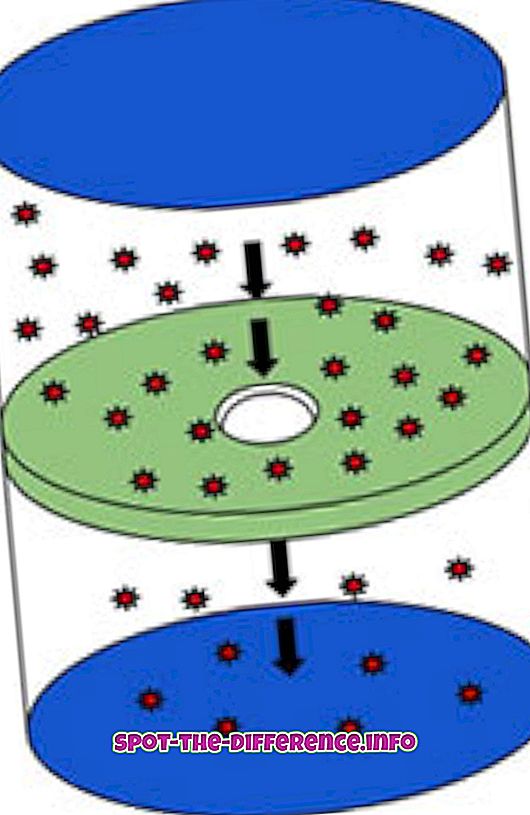
Az effúzió az a folyamat, amellyel a molekulák egy nagy lyukú helyről alacsony koncentrációra haladnak. Az eljárás a gáz azon képességét írja le, hogy a molekulák közötti ütközések nélkül egy kis lyukon haladjon. Ez akkor fordul elő, ha a lyuk átmérője lényegesen kisebb, mint a molekulák átlagos szabad útja. Az átlagos szabad utat a mozgó részecske által megtett átlagos távolság az egymást követő ütközések között. Ennek gyakorlati példája az, ha egy tartályt töltünk egy üvegbe füsttel és egy kis lyukat a palackban, és a füst, amely a lyukból kiindul, elfolyásnak minősül.
A skót kémikus szerint Thomas Graham, aki létrehozta az effúzió mérésére szolgáló képletet, létrehozott egy Graham törvényt, amely meghatározza, hogy a gáz milyen gyorsan utazik és hogyan mérhető. Graham törvénye szerint a gázok kibocsátási sebessége a molekulatömegtől függ. Az alacsonyabb molekulatömegű gáz gyorsabban kiürül, mint a nagyobb molekulatömegű gáz. Az effúziót úgy számítjuk ki, hogy mérjük, hogy hány molekula halad át a lyukon egy másodperc alatt. Hasonlóképpen a termodinamikában a gáz effúzió sebessége fordítottan arányos a részecskék tömegének négyzetgyökével.