Főbb különbség: A molaritás, amit moláris koncentrációnak is neveznek, mért értékét méri az egy liter oldatban lévő anyagra. A molaritás tőkével van jelölve. M. Molality méri az anyag jelenlétének számát egy kilogramm oldószerben. A molalitást egy kis m betű jelöli.
Mindkét koncepció számításai alapján megállapítható, hogy hány mól van jelen a jelenlegi megoldásban. Az oldatot homogén keverékként definiálhatjuk, ami azt jelenti, hogy két vagy több komponenst összekeverünk azzal a ponttal, hogy szabad szemmel nem lehet megkülönböztetni. Ez a két fogalom megérti a mólokat, mivel meghatározza az oldatban jelen lévő molok számát. Az olasz tudós, Amedeo Avogardo felfedezte a mólok elméletét.
1811-ben Avogardo azt javasolta, hogy a gáz térfogata egy adott hőmérsékleten és nyomáson arányos legyen az atomok vagy molekulák számával, függetlenül a természetétől. Ezt az elképzelést Avogardo állandónak nevezik. Ez az összetevő részecskék (általában atomok vagy molekulák) száma egy adott anyag egy moljában. A mesterséges értelemben az anyag egy mólja képviseli az elemben jelen lévő atomok és molekulák számát. Például: Az oxigén atomtömege 16, ez az oxigén móljára vonatkoztatva. Tehát egy mól oxigén tömege 16 gramm lenne. Avogardo szerint egy mól oxigén ugyanolyan számú atommal rendelkezne, mint egy mól hidrogén. Ezek azonban eltérhetnek a súlytól.
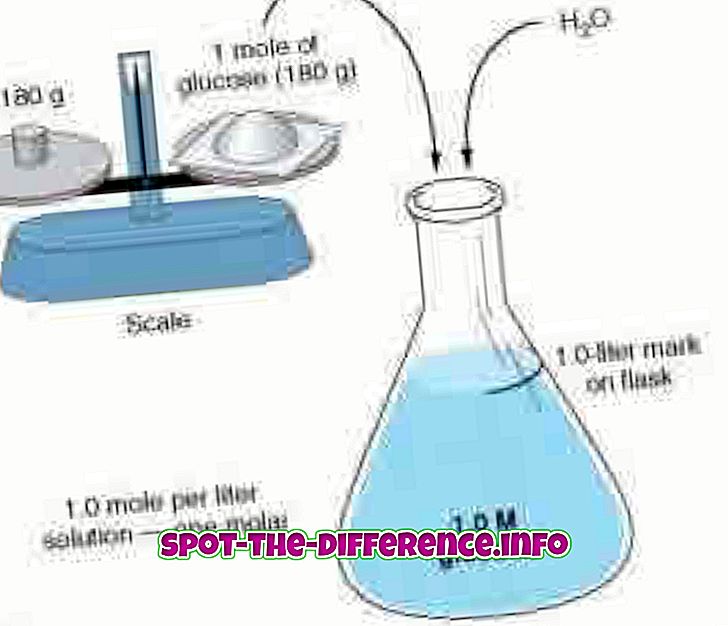
A molaritás és a molalitás két különböző megközelítéssel méri a koncentrációt. A moláris koncentráció, más néven mólkoncentráció, mért értékét méri az anyag literben kifejezve. A molaritás tőke M.-vel van jelölve. Tehát egy 1, 0 M-os megoldás azt jelzi, hogy 1 mól oldatot tartalmaz 1 liter oldatban. Például: víz és cukor oldat. Ha az oldatot 1, 0 M-ban mérjük, akkor az oldat 1 mól cukrot tartalmaz a jelenlévő oldat literenként. A molaritás az anyag koncentrációjának, a koncentrációnak, az anyagkoncentrációnak vagy egyszerűen a koncentrációnak is nevezik. A molaritás kiszámítható az alábbi képlettel: M = mol (mol mól / l) (az oldat térfogata literben).

A molalitás méri az anyag jelenlétét az oldószer kilogrammonként. A molalitást egy kis m betű jelöli. Tehát egy 1, 0 m-es megoldás azt jelzi, hogy 1 mól oldott anyagot tartalmaz az oldószer kilogrammonként. Válasszuk ki az oldott anyagot az oldószerrel. Az oldható anyag az anyag, amely egy másik anyagba oldódik. Az oldószer olyan anyag, amely feloldja az oldott anyagot. Tehát, ha a vizet és a cukrot összekeverik, a cukor az oldott anyag és az oldószer víz. A kevert cukor víz lenne a megoldás. Most már a molalitás szempontjából rendkívül fontos, hogy a mólokat az oldószer tömegével és nem az oldattal osztjuk meg. A molalitás a következő képlettel számítható: m = mol (mol mól) / KG (az oldószer tömege kg-ban).
Miért a különbség? Nos, mindkettőt a hőmérséklet kezelésére használják. Ha egy oldat változik a hőmérsékleten, akkor molalitást alkalmazunk. Azonban a konstans hőmérsékleten maradó megoldásoknál a molaritás kerül alkalmazásra. Ennek oka, hogy a hőmérséklet emelkedése vagy csökkenése esetén az oldat térfogata megváltozik, és ez közvetlenül befolyásolja a molaritást. Ezért a koncentráció kiszámításához molalitást használunk.