A legfontosabb különbség: Az atomok elhelyezkedése egy molekulában segít meghatározni annak polaritását. Egy molekula polárisnak mondható, ha pozitív és negatív töltéssel rendelkezik. A nem poláris molekula kisebb töltéssel rendelkező molekula.
A kémia területén a polaritás egy elektromos dipólusú vagy többpólusú pillanatú molekula vagy vegyi csoport elektromos töltéseinek elválasztását jelenti. A poláris molekulák intermolekuláris kötéseken és hidrogénkötéseken keresztül hatnak egymásra. A molekuláris polaritás az molekulában lévő atomok közötti elektronegativitás különbségétől függ. A polaritás azt is meghatározza, hogy számos fizikai tulajdonság, például a felületi feszültség, az olvadás és a forráspontok, valamint az oldhatóság.
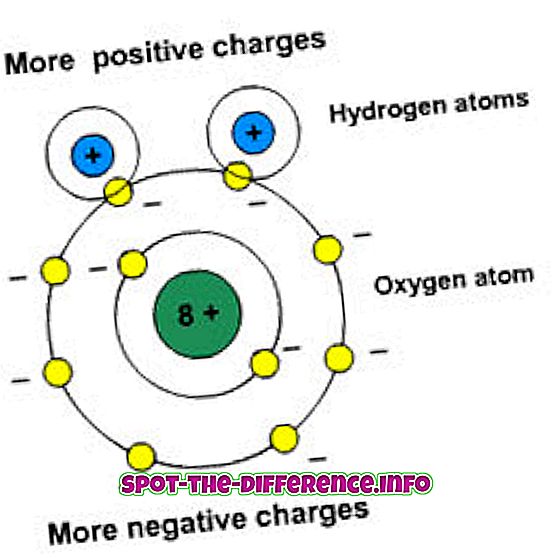
A polaritás a díjak elválasztását jelenti. Ezeknek a molekuláknak van egy dipol pillanatuk. A Dipol pillanat méri a kötés polaritását. A poláris anyagok kölcsönhatásba lépnek más poláris elemekkel.

A nem poláris molekula nem rendelkezik elegendő töltéssel. A nem-poláris molekulák szimmetrikus módon oszlanak el, és nem rendelkeznek nagyszámú elektromos töltéssel. Ha két atomnak vagy két azonos atomnak van azonos elektronkötése közöttük, akkor az atomok az elektronpárot húzzák. Ez a húzás segít nekik megosztani az elektronokat, és ez a fajta kötésmegosztás a molekulák között nem poláros kovalens kötésekként ismert.
Polar és nem poláris összehasonlítás:
Poláris | Nem Polar | |
Meghatározás | A poláris anyagok pozitív és negatív töltéssel rendelkeznek az atomon. | A nem poláris anyagoknak nincs nagy töltése az atomhoz. |
Mozgalom | Elektromos dipolmozgással rendelkeznek. | Nem rendelkeznek dipol mozgással. |
Töltési elválasztás | Van töltés elválasztás. | Nincs külön díj. |
Interakció | Más poláris anyagokkal kölcsönhatásba lépnek. | Nem hatnak más poláros anyagokkal. |
Példa | Víz, alkohol és kén. | Olaj. |