Kulcskülönbség: Az abszorpció egy olyan nagyfokú jelenség, amelyben az abszorbens teljesen behatol egy szilárd vagy folyékony testbe egy vegyület vagy oldat létrehozásához. Másrészt az adszorpció olyan felületjelenség, amelyben az adszorbátum molekulái csak egy adszorbens felületén koncentrálódnak.
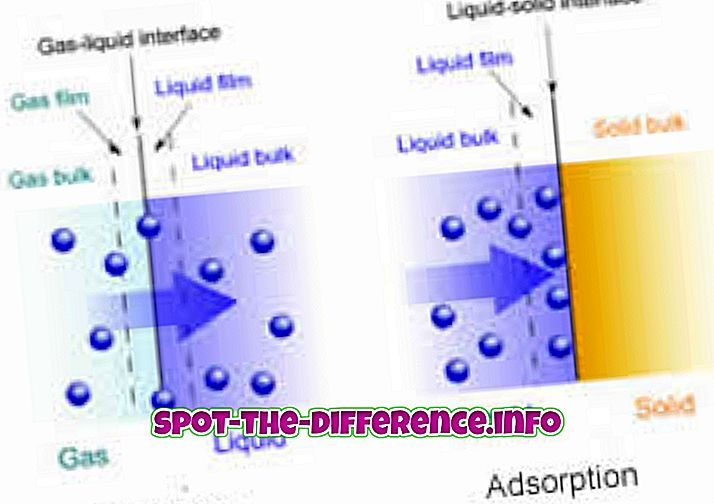
Kémiai reakció - kálium-szén oldattal elnyelt szén-dioxid
Fizikai folyamat - A vízben oldódó levegő felszívódik

Kétféle adszorpciós mód van - kémiai és fizikai. Kémiai adszorpció esetén a molekulákat és a felületet gyenge Vander Walls erők kötik össze. Másrészt a kémiai adszorpció során a molekulák és a felület között kémiai kötés jön létre.
Ezért az adszorpció és az abszorpció között az elsődleges különbség az, hogy az abszorpció nagy mennyiségű jelenség, ami azt jelenti, hogy az anyag teljes testén történik, míg az adszorpció felületi jelenség. Az adszorpció mindig exoterm, míg az abszorpció endoterm. A szorpció magában foglalja mind az abszorpciós, mind az adszorpciós folyamatokat.
Az adszorpció és az abszorpció összehasonlítása:
Adszorpció | Abszorpció | |
defintion | Gáz vagy folyékony anyag felhalmozódása szilárd vagy folyékony felületre | Egy anyag folyékony vagy szilárd anyagba való diffúziója oldatot vagy vegyületet képez |
Példa | Inert gázok adszorbeálódnak a szénen. | A száraz szivacs elnyeli a vizet |
Hőcsere | Exotermikus, kivéve a H2 adszorpcióját üvegre | endoterm |
Egyensúly elérése | Összehasonlítva gyorsabb | Összehasonlítva lassan |
koncentráció | Az adszorbens felületén való koncentráció eltér az ömlesztett anyagtól | A koncentráció az anyag egészében változatlan marad |
Előfordulási arány | Kezdetben gyors, de később csökken az aránya | Egységes arányban történik |